王雁玲组
生殖病理学研究组的前身是庄临之研究员带领的“细胞与分子生物学研究组”。2007年更名为“生殖病理学研究组”,致力于研究胎盘发育和妊娠适应性调控的分子机理,并以此为切入点研究子痫前期和复发流产等重大妊娠疾病的发病机制。
哺乳动物的妊娠起始于成熟囊胚的滋养层细胞与子宫内膜识别、黏附,并进一步向子宫内膜侵袭,将胚胎牢固地锚定在子宫壁上。伴随胚胎发育,胚胎滋养层细胞活跃增殖和分化,对子宫内膜基质和螺旋动脉进行改建和重构,建立完善的胎盘-子宫血液循环。因而,胎盘发育是哺乳动物妊娠成功建立和维持的重要保障。胎盘发育不完善将引起一系列复杂的妊娠相关疾病,如子痫前期、复发流产、胎儿生长受限等,对妊娠妇女、胎儿的健康乃至出生人口的远期发育都造成严重危害。
迄今,对人类胎盘的认识依然是个“黑匣子”,其发育调控机理及其介导的母体妊娠适应性调节机制仍有待阐明,而与之密切相关的妊娠重大疾病的预测、防治和干预也亟待突破。
针对上述科学问题,我们的主要研究内容是:
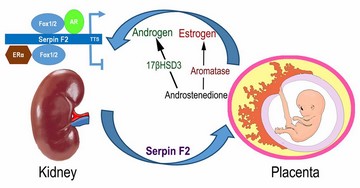
1) 阐释胎盘与母体脏器之间协同适应的妊娠适应性调节机制;
2) 基于子痫前期特异标志分子的挖掘,研究HGF/c-Met信号、mTOR信号及多种microRNAs在胎盘发育中的调控作用;
3) 以蜕膜NK细胞(dNK)为主,研究母胎界面多细胞互作的分子基础,阐释复发流产和子痫前期的免疫失衡发病机制;
4) 发展子痫前期和复发流产等重要妊娠疾病的综合预测和干预策略。
我们已经建立和稳定了包括不同分化程度的人滋养层细胞原代培养和永生化细胞系、胎盘外植体培养、滋养层细胞-血管内皮细胞-dNK细胞互作、小鼠滋养层干细胞培养和分化等体外研究模型,并稳定了CYP19-Cre介导或慢病毒/腺病毒介导的胎盘特异基因敲除/敲降或过表达的小鼠模型。通过与多中心临床单位协作,建立了子痫前期等妊娠重要疾病前瞻性标本库;获得了一批可用于子痫前期早期诊断的分子标志物。阐释了Activin/Nodal信号、HGF/c-Met信号以及多种microRNAs的功能和调节障碍干扰胎盘滋养层细胞功能,并引发子痫前期发生发展的分子机制。进一步地,我们将从妊娠适应性调节和免疫调控的角度深入探讨胎盘发育和妊娠维持的机理,全面阐述胎盘与母体器官之间协同适应的妊娠适应性调节与子痫前期和复发流产等疾病的分子关联。期待通过基础与临床相结合的研究,揭开人类胎盘发育和妊娠维持调控的神秘面纱,并为发展重要妊娠疾病的预测和干预策略奠定坚实的科学基础。